Psykopatologi, metabolisme og livskvalitet hos patienter med første-episode psykose
Betydningen af mental og fysisk sundhed for livskvaliteten hos patienter, der debuterer med psykose, er stadig ikke tilstrækkeligt afdækket. I denne artikel præsenteres resultaterne fra et studie, der afdækkede, hvordan mental og fysisk sundhed påvirker livskvaliteten før og efter antipsykotisk behandling.
Traditionelt set har forskningen i og behandlingen af patienter med skizofreni fokuseret på at lindre psykotiske, såkaldte positive symptomer, herunder hallucinationer, formelle tankeforstyrrelser og vrangforestillinger. Som led i psykiatriens af-institutionalisering op igennem 1960’erne og 1970’erne fremkom imidlertid et øget fokus på at forbedre livskvaliteten hos patienter med svære psykiske lidelser som led i patienternes integration i samfundet1. Det blev desuden i stigende grad anerkendt, at de ofte mindre åbenlyse negative symptomer såsom apati, manglende motivation og social isolation har stor betydning for sygdomsforløbet2.
Livskvalitet
Antipsykotika og dysmetabolisme
Antipsykotisk medicin har veldokumenterede effekter, når det kommer til behandling af positive symptomer; dog er virkningen på negative symptomer mindre konsistent. Antipsykotika er potente lægemidler, og bivirkninger i form af vægtøgning og dysmetabolisme er almindeligt kendte kliniske udfordringer3,4. Yderligere kompliceres billedet af, at genetiske, miljømæssige og livsstilsrelaterede faktorer også disponerer patienter med skizofreni til at have og/eller udvikle metaboliske forstyrrelser såsom nedsat insulinfølsomhed og øget legemsvægt selv før opstart af antipsykotika5,6. Metabolisk syndrom (MetS) er en samling risikofaktorer, herunder central fedme, dyslipidæmi, forhøjet blodtryk og hyperglykæmi, der øger risikoen for kardiovaskulær sygdom7. Prævalensen af MetS hos patienter med første-episode psykose (FEP) er estimeret til 10%8. Til sammenligning er prævalensen af MetS hos raske unge estimeret til 7%9. Desuden viser studier, at unge, antipsykotika-naive patienter med FEP er særligt sårbare over for at tage på i vægt efter opstart af antipsykotisk behandling10.
Livskvalitet hos patienter med første-episode psykose – hvad ved vi?
Betydningen af metaboliske komorbiditeter på livskvaliteten er primært blevet undersøgt hos patienter med længerevarende skizofreni, hvor bl.a. vægtøgning og øget Body Mass Index (BMI) er blevet associeret med lavere livskvalitet11,12. For patienter med FEP fandt en nylig pilotundersøgelse, at livskvaliteten tilsyneladende ikke blev påvirket af antipsykotika-relaterede bivirkninger13. Dog vanskeliggør antallet af patienter i undersøgelsen muligheden for at drage sikre konklusioner. Undersøgelser af patienter med FEP har desuden vist, at negative symptomer i højere grad påvirker livskvaliteten end positive symptomer, og at længere varighed af ubehandlet psykose er forbundet med nedsat livskvalitet14.
Sværere grad af positive symptomer samt øget livvidde var associeret med lavere tilfredshed med boligsituation, mens en sværere grad af negative symptomer var associeret med en lavere tilfredshed med sociale relationer og selvopfattelse/nuværende livssituation.
Prædiktorer for livskvalitet
Formålet med dette studie var at undersøge sammenhængen mellem psykopatologi, metabolisme og livskvalitet hos antipsykotika-naive patienter med FEP i alderen 18-45 år før og efter antipsykotisk behandling. Studiet blev udført som en longitudinel, observationel kohorteundersøgelse med data fra PECANS I- og PECANS II-kohorterne15,16 (Figur 1). Graden af symptomer blev vurderet ved hjælp af Positive and Negative Syndrome Scale (PANSS)17. Prævalensen af MS blev bestemt ud fra den seneste definition fra International Diabetes Federation (IDF)18. Livskvalitet blev vurderet ud fra Satisfaction with Life Scale (SWLS)19, et selvrapporteret spørgeskema, der måler subjektiv livskvalitet i fire domæner; boligsituation, sociale relationer, selvopfattelse/nuværende livssituation og arbejdssituation. Multipel lineær regression blev anvendt som statistisk metode til at identificere potentielle prædiktorer for livskvalitet ved baseline og efter seks uger. Vi konstruerede forskellige modeller, der hver især fokuserede på et specifikt domæne af livskvalitet. De endelige modeller blev udvalgt på baggrund af deres indbyrdes Akaike Information Criterion (AIC) score; en score, der lidt forenklet sagt, udvælger den/de enkleste model(ler), der bedst forklarer data. Desuden blev hver af de udvalgte modeller kontrolleret for alder og køn. Endelig anvendte vi data fra raske kontroller uden psykisk lidelse fra FOCUS-studiet20 i en deskriptiv post hoc-analyse, hvor vi sammenlignede BMI ved baseline mellem patienter og raske kontroller.

Høj prævalens af metabolisk syndrom
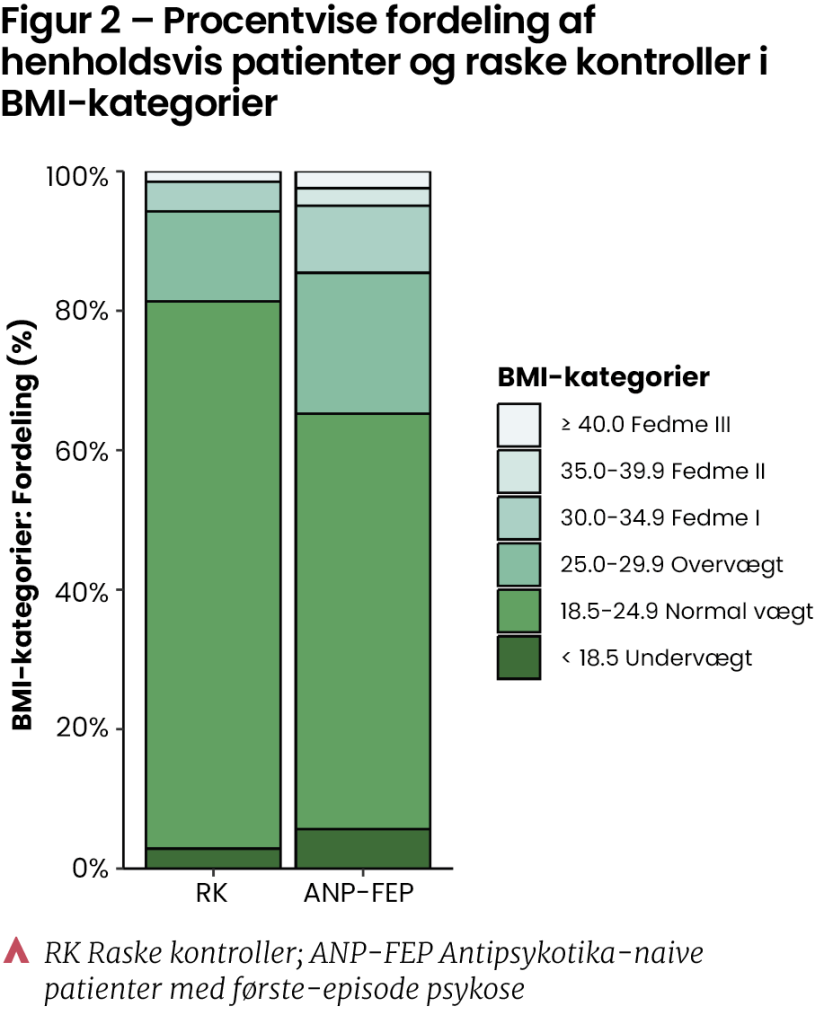
I alt blev 125 patienter (46% kvinder) undersøgt ved baseline med en aldersmedian på 22.7 år (range 18.2; 42.6). Efter seks ugers initial antipsykotisk monoterapi med enten amisulprid (mediandosis ved follow-up = 200 mg) eller aripiprazol (mediandosis ved follow-up = 10 mg), blev 89 patienter (47% kvinder) genundersøgt. Før opstart af antipsykotisk behandling opfyldte 22 af patienterne (19.3%) kriterierne for MetS, hvilket er en høj prævalens sammenlignet med tidligere studier8,21,22. Efter seks ugers behandling blev 15 af disse patienter genundersøgt, hvoraf 10 af patienterne stadig opfyldte kriterierne for MetS. Yderligere havde fire patienter udviklet MetS i løbet af de seks uger. Desuden sås en signifikant stigning i både kropsvægt på 1.3 kg og BMI på 0.4 kg/m2. Post hoc-analysen viste, at antallet af patienter i BMI-kategorierne overvægt/fedme var omtrent dobbelt så stort sammenlignet med antallet af raske kontroller (Figur 2). Dette kan imidlertid afspejle den stigende prævalens af overvægt og fedme i europæiske lande23, dog med større variation i fordelingen af patienter i forskellige BMI-kategorier. Det vil sige flere patienter repræsenteret i ekstremerne (undervægt, fedme klasse I, II og III).
Graden af psykopatologi er afgørende for livskvaliteten
Efter seks ugers behandling kunne vi observere en signifikant stigning i livskvalitet i domænerne sociale relationer og selvopfattelse/nuværende livssituation, samt et signifikant fald i både positive og negative symptomer. Ved baseline viste regressionsanalyserne, at en sværere grad af positive symptomer samt øget livvidde var associeret med lavere tilfredshed med boligsituation, mens en sværere grad af negative symptomer var associeret med en lavere tilfredshed med sociale relationer og selvopfattelse/nuværende livssituation. Det samme billede gjorde sig gældende efter seks uger. Resultaterne fra dette studie antyder, at i de tidlige stadier af antipsykotisk behandling har metaboliske forstyrrelser mindre indflydelse på livskvaliteten end sværhedsgraden af symptomer. Det er dog vigtigt at understrege, at hverken amisulprid eller aripiprazol hører til de antipsykotika, der er stærkest forbundet med metaboliske bivirkninger. Ikke desto mindre ordineres begge lægemidler ofte i klinisk praksis, især til patienter, der ikke tidligere har fået antipsykotika. Derudover er unge og antipsykotika-naive patienter generelt mere følsomme over for udvikling af antipsykotika-induceret vægtøgning, og dette kan forekomme både med amisulprid og aripiprazol24,25,27.
Konklusion
Sværhedsgraden af psykopatologi påvirker direkte livskvaliteten både før og efter behandling. Metabolismeforstyrrelser har umiddelbart en mindre betydning for livskvaliteten i de tidlige stadier af antipsykotisk behandling. Endelig understreger resultaterne den tætte forbindelse mellem psykotiske lidelser og dysmetabolisme i form af høj prævalens af MetS samt forværring af dysmetabolismen allerede ved den indledende antipsykotiske behandling.
-
Referencer
- National Institute of Mental Health. Deinstitutionalization: An analytical review and sociological perspective. DHEW Publ. 1976;No. (ADM):76-351.
- Foussias G, Agid O, Fervaha G, Remington G. Negative symptoms of schizophrenia: Clinical features, relevance to real world functioning and specificity versus other CNS disorders. Eur Neuropsychopharmacol [Internet]. 2014 [cited 2022 Dec 13];24(5):693-709. Available from: http://dx.doi.org/10.1016/j.euroneuro.2013.10.017
- Tschoner A, Engl J, Laimer M, Kaser S, Rettenbacher M, Fleischhacker WW, et al. Metabolic side effects of antipsychotic medication [Internet]. Vol. 61, International Journal of Clinical Practice. 2007 [cited 2022 Nov 1]. p. 1356-70. Available from: https://onlinelibrary.wiley.com/doi/10.1111/j.1742-1241.2007.01416.x
- Dumontaud M, Korchia T, Khouani J, Lancon C, Auquier P, Boyer L, et al. Sexual dysfunctions in schizophrenia: Beyond antipsychotics. A systematic review. Prog Neuropsychopharmacol Biol Psychiatry [Internet]. 2020;98:109804. Available from: https://doi.org/10.1016/j.pnpbp.2019.109804
- Tomasik J, Lago SG, Vázquez-Bourgon J, Papiol S, Suárez-Pinilla P, Crespo-Facorro B, et al. Association of insulin resistance with schizophrenia polygenic risk score and response to antipsychotic treatment. JAMA Psychiatry. 2019;76(8):864-7.
- Manu P, Dima L, Shulman M, Vancampfort D, De Hert M, Correll CU. Weight gain and obesity in schizophrenia: Epidemiology, pathobiology, and management. Acta Psychiatr Scand. 2015;132(2):97-108.
- Mottillo S, Filion KB, Genest J, Joseph L, Pilote L, Poirier P, et al. The metabolic syndrome and cardiovascular risk: A systematic review and meta-analysis. J Am Coll Cardiol. 2010;56(14):1113-32.
- Nyboe L, Vestergaard CH, Moeller MK, Lund H, Videbech P. Metabolic syndrome and aerobic fitness in patients with first-episode schizophrenia, including a 1-year follow-up. Schizophr Res [Internet]. 2015 [cited 2023 Jan 23];168(1-2):381-7. Available from: http://dx.doi.org/10.1016/j.schres.2015.07.053
- Nolan PB, Carrick-Ranson G, Stinear JW, Reading SA, Dalleck LC. Prevalence of metabolic syndrome and metabolic syndrome components in young adults: A pooled analysis. Prev Med Reports. 2017 Sep 1;7:211-5.
- Smith E, Singh R, Lee J, Colucci L, Graff-Guerrero A, Remington G, et al. Adiposity in schizophrenia: A systematic review and meta-analysis. Acta Psychiatr Scand [Internet]. 2021 Dec 1 [cited 2022 Nov 3];144(6):524-36. Available from: https://onlinelibrary-wiley-com.ep.fjernadgang.kb.dk/doi/full/10.1111/acps.13365
- Allison DB, Mackell JA, McDonnell DD. The impact of weight gain on quality of life among persons with schizophrenia. Psychiatr Serv. 2003;54(4):565-7.
- Faulkner G, Cohn T, Remington G, Irving H. Body mass index, waist circumference and quality of life in individuals with schizophrenia. Schizophr Res [Internet]. 2007 [cited 2022 Oct 25];90(1-3):174-8. Available from: www.elsevier.com/locate/schres
- Chintoh A, Agarwal M, Mackenzie N, Remington G, Hahn M. T231. QUALITY OF LIFE IN ANTIPSYCHOTIC-NAïVE YOUTH: EXPLORING THE INTERPLAY WITH METABOLIC SIDE-EFFECTS. Schizophr Bull. 2020 May 18;46(Suppl 1):S321.
- Watson P, Zhang JP, Rizvi A, Tamaiev J, Birnbaum ML, Kane J. A meta-analysis of factors associated with quality of life in first episode psychosis. Schizophr Res. 2018 Dec 1;202:26-36.
- Nielsen MO, Rostrup E, Wulff S, Bak N, Broberg BV, Lublin H, et al. Improvement of brain reward abnormalities by antipsychotic monotherapy in schizophrenia. Arch Gen Psychiatry [Internet]. 2012 Dec 1 [cited 2023 Jan 11];69(12):1195-204. Available from: https://jamanetwork.com/journals/jamapsychiatry/fullarticle/1263991
- Bojesen KB, Ebdrup BH, Jessen K, Sigvard A, Tangmose K, Edden RAE, et al. Treatment response after 6 and 26 weeks is related to baseline glutamate and GABA levels in antipsychotic-naïve patients with psychosis. Psychol Med [Internet]. 2020 Oct 1 [cited 2023 Jan 11];50(13):2182-93. Available from: https://www.cambridge.org/core/journals/psychological-medicine/article/treatment-response-after-6-and-26-weeks-is-related-to-baseline-glutamate-and-gaba-levels-in-antipsychoticnaive-patients-with-psychosis/50C770EFC615E301D9537DC5A9456024
- Kay SR, Fiszbein A, Opler LA. The positive and negative syndrome scale (PANSS) for schizophrenia. Schizophr Bull. 1987;13(2):261-76.
- Alberti KGMM, Zimmet P, Shaw J. Metabolic syndrome - A new world-wide definition. A consensus statement from the International Diabetes Federation. Diabet Med. 2006;23(5):469-80.
- Test MA, Greenberg JS, Long JD, Brekke JS, Burke SS. Construct validity of a measure of subjective satisfaction with life of adults with serious mental illness. Psychiatr Serv [Internet]. 2005 Mar 1 [cited 2022 Oct 11];56(3):292-300. Available from: https://ps.psychiatryonline.org/doi/10.1176/appi.ps.56.3.292
- Wenneberg C, Nordentoft M, Rostrup E, Glenthøj LB, Bojesen KB, Fagerlund B, et al. Cerebral glutamate and gamma-aminobutyric acid levels in individuals at ultra-high risk for psychosis and the association with clinical symptoms and cognition. Biol Psychiatry Cogn Neurosci Neuroimaging [Internet]. 2020;5(6):569-79. Available from: https://doi.org/10.1016/j.bpsc.2019.12.005
- Fleischhacker WW, Siu CO, Bodén R, Pappadopulos E, Karayal ON, Kahn RS. Metabolic risk factors in first-episode schizophrenia: Baseline prevalence and course analysed from the European First-Episode Schizophrenia Trial. Int J Neuropsychopharmacol [Internet]. 2013 [cited 2023 Jan 27];16(5):987-95. Available from: https://academic.oup.com/ijnp/article/16/5/987/715721
- Garrido-Torres N, Rocha-Gonzalez I, Alameda L, Rodriguez-Gangoso A, Vilches A, Canal-Rivero M, et al. Metabolic syndrome in antipsychotic-naïve patients with first-episode psychosis: A systematic review and meta-analysis [Internet]. Vol. 51, Psychological Medicine. 2021 [cited 2023 Feb 4]. p. 2307-20. Available from: https://doi.org/10.1017/S0033291721002853
- WHO Regional office for Europe. WHO European Regional Obesity Report 2022 [Internet]. 2022 [cited 2023 Feb 3]. 1-220 p. Available from: http://apps.who.int/bookorders.
- Ebdrup BH, Knop FK. Weight gain on antipsychotics – A perfect storm of complex pathophysiology and psychopharmacology [Internet]. Vol. 144, Acta Psychiatrica Scandinavica. John Wiley & Sons, Ltd; 2021 [cited 2022 Nov 3]. p. 521-3. Available from: https://onlinelibrary-wiley-com.ep.fjernadgang.kb.dk/doi/full/10.1111/acps.13376
- Correll CU, Manu P, Olshanskiy V, Napolitano B, Kane JM, Malhotra AK. Cardiometabolic risk of second-generation antipsychotic medications during first-time use in children and adolescents. JAMA [Internet]. 2009 Oct 28 [cited 2022 Nov 3];302(16):1765-73. Available from: https://jamanetwork-com.ep.fjernadgang.kb.dk/journals/jama/fullarticle/184782
- The WHOQOL Group. The World Health Organization quality of life assessment (WHOQOL): Position paper from the World Health Organization. Soc Sci Med. 1995;41(10):1403-9.
- ter Hark SE, Jamain S, Schijven D, Lin BD, Bakker MK, Boland-Auge A, et al. A new genetic locus for antipsychotic-induced weight gain: A genome-wide study of first-episode psychosis patients using amisulpride (from the OPTiMiSE cohort). J Psychopharmacol. 2020;34(5):524–31.
-
Interessekonflikter
AD var finansielt støttet af Lundbeckfondens scholarstipendiat. BE har været tilknyttet Advisory Boards for Eli Lilly Danmark A/S, Janssen-Cilag, Lundbeck Pharma A/S og Takeda Pharmaceutical Company Ltd og har modtaget foredragshonorarer fra Bristol-Myers Squibb, Boehringer Ingelheim, Otsuka Pharma Scandinavia AB, Eli Lilly Company og Lundbeck Pharma A/S. The Centre for Clinical Intervention and Neuropsychiatric Schizophrenia Research (CINS) er støttet af Lundbeckfonden, bevillingsnummer R25-A2701. De øvrige forfattere erklærer ingen interessekonflikter.
Brænder du for at skrive?
Vil du gerne dele din forskning eller dine kliniske erfaringer med dine kollegaer inden for netop dit speciale? Har du en ide til en artikel, som du gerne vil udgive hos os? Send redaktionen en mail på redaktion@bpno.dk
Send mail til redaktionen









